溶液的界限 : 摩尔力, 摩尔和摩尔分数
章溶液的界面性质包括对摩尔的解释, 摩尔和摩尔分数

理解解决方案的界面性质
“解决方案的界面性是 溶液的性质不取决于溶质的类型,而取决于溶质颗粒的浓度”
该解决方案的界面特性由两种类型组成, 即电解质溶液的相结合特性以及非电解质溶液的相关特性
摩尔力, 摩尔和摩尔分数
在解决方案中, 由溶质颗粒数量确定的物质的几种特性]. 溶液的界限特性取决于溶质颗粒的数量, 请记住解决方案的集中度
摩尔力 (m)
摩尔力是大量溶质的摩尔 1 升解决方案.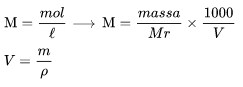
信息 :
m是摩尔力
MR是溶质摩尔的质量
v是解决方案的体积,
摩尔 (m)
摩尔特是溶质中的摩尔数量 1 公斤 (1000 克) 溶剂.
摩尔特是由方程定义的:![]()
信息:
m是摩尔 (mol/kg)
MR是溶质摩尔的质量 (g/mol)
质量是溶质的质量 (g)
p是溶剂的质量 (g)
摩尔派
摩尔分数是基于摩尔的所有组分的浓度单位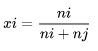
非电解质溶液的综合性能
综合性能涉及溶液, 相结合特性不取决于溶剂分子和溶质的相互作用, 但是卡在溶液中的溶质量.
相结合特性由 :
- 减轻蒸汽压力
- 沸点增加
- 冰点下降
- 渗透压
减轻蒸汽压力
![]()
P0 =纯液体蒸气压
p =蒸汽溶液
沸点增加
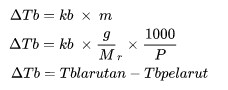
ΔTB 是沸点的增加 (OC)
KB 是摩尔沸点的恒定增加
m 是溶液的摩尔性 (mol/kg)
先生 是相对分子的质量
p 是物质的质量 (公斤)
沸点增加恒定表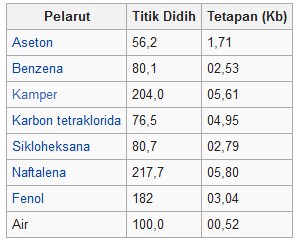
冰点下降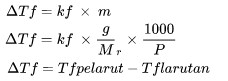
ΔTF 是冰点的减少 (OC)
KF 是冷冻点的设置 (OC KG/mol)
m 是溶液的摩尔性 (mol/kg)
先生 是相对分子的质量
p 是物质的质量 (公斤
渗透压
Π = m × r × t
Π 是渗透压
m 是溶液的摩尔力
r 是气体设置 (0,082)
t 是绝对温度
电解质溶液的界限
在相同的浓度下, 电解质溶液的界面特性比非电解质溶液的界面特性更大. 电解质溶液的电离反应中溶质的颗粒数量是配制的。
i = 1 + (n − 1) α
信息 :
我是货车不是霍夫因素
n是阳离子系数的数量
α 是电离的程度
饱和蒸气压力降低
ΔP = P0 × x t e r l a r u t × 我
沸点增加
Δ t b = k b × m × 我
冰点下降
Δtf = k f × m × 我
渗透压
π = m × r × t × 我
因此,讨论解决方案的界面性质, 希望有用
其他文章 :
- 几何公式和几何序列示例
- 病毒 : 结构, 分类, 形式, 病史的历史和理解和例子
- 磁场 : 特征, 理解和公式
解决方案的后界性特性 : 摩尔力, 摩尔和痣派别首先出现在此页面上.