氧化还原和电化学反应 : 理解和示例
氧化还原和电化学反应

理解
化学反应可以分为各种反应. 其中之一是与反应前后原子的氧化数变化有关的反应.
从对反应氧化数的综述可以分为 2 键入即 :
反应组涉及的原子在反应之前或之后没有经历氧化数的变化. 所涉及的原子不经历氧化数变化的反应称为非还原氧化反应,通常称为 反应不是氧化还原.
反应组涉及的原子经历了氧化数的变化. 涉及原子的氧化数量之前或之后,涉及的原子数不相同 (改变了). 该反应称为还原氧化反应 (氧化还原反应)
氧化还原反应的定义
重新多 (还原氧化). 还原是电子接收或氧化数量减少, 而氧化是电子的释放或氧化数的增加
例子 还原反应
Cu2+(aq) + 2e ® 铜 (s) Ag+(aq) + e ® Ag(s)
例子 氧化反应
Zn(s) ® Zn2+(aq)+ 2和al(s) ® Al3+(aq) + 3e
确定氧化数的规则 :
- 元素中的原子原子具有许多无效的氧化
- 原子h在一个圆锥状的氧化中有多种氧化 +1
- 金属氢化物 (例如,很好, bah2, Alh3) h数与 -1
- F2O化合物, 氧化数O = +2
- 在过氧化物中 (H2O2, Na2O2, BaO2) o氧化数等于 -1
- 该化合物中的金属原子具有阳性的氧化数量
- 该化合物中的原子氧化数量等于零
- 离子中原子的氧化数量与离子电荷相同
- 如果两个原子结合, 负氧化数总是由电负性趋于更大的原子所有
氧化还原基本概念
- 氧化是电子释放事件或氧化数量的添加
- 还原是电子捕获事件或氧化数量减少
- 减速器 (减少) 是一种正在释放电子的物质的物质, 或氧化数量往往会上升的物质
- 氧化剂是减少或捕获电子物质的物质 / 氧化数量下降的物质
- 氧化还原是一种由还原和氧化或氧化变化反应组成的反应
- 比例反应 (破裂) 是一种氧化还原反应,其中仅减少一种原子,氧化或氧化还原反应,这只是一种原子,其氧化数变化
- 电子摩尔是氧化数之间的差异
氧化数法
反应均衡步骤 :
- 根据每个元素的氧化数变化,确定经历氧化和还原的元素
- 通过添加适当的系数来均衡体验氧化还原的元素数量
- 确定经历氧化数量变化的元素的氧化数量增加或减少
- 通过给出适当的系数来表达氧化数的变化
- 均衡H和O原子的数量以及其他元素
一半反应方法
反应均衡步骤:
写有氧化还原反应的物质
将反应分为两个, 还原反应的一半和一半的氧化反应
均衡体验氧化还原的原子, 除了氢原子 (h) 和氧气 (o)
通过在氧缺乏段中添加H2O分子来为氧原子配置
通过将H+离子添加到缺乏原子h的段来配备氢原子
通过将电子添加到具有更正电荷的部分来均衡电荷
将电子数量等同于两个方程的减少和氧化反应的一半
将反应一半的两个方程组合在一起,成为整个氧化还原反应
以初始反应的形式恢复
电化学细胞的定义
溶液中的氧化还原反应中的电子转移是通过原子形式的直接接触颗粒之间的直接接触 , 互相授予的分子或离子.
电化学细胞是一个细胞或位置,其中电子流是由化学能量变化到电能引起的,反之亦然. 该单元组分为两种,即 :
- SEL VAULT
- 电解细胞
伏尔塔细胞涉及化学能的变化到电能,而电解细胞涉及电能变化到化学能. 该过程如何发生?
SEL VAULT
SEL VAULT 利用自发反应 (∆g < 0) 产生电能, 反应能量与产品的差异被转换为电能. 反应系统确实在环境中起作用
电解细胞 利用电能执行非庞然反应 (∆g > 0) 系统的工作环境
两种类型的电池都使用电极, 即在电池和环境之间进行电力并浸入电解质的物质 (离子混合物) 参与反应或携带电荷的.
伏特细胞成分
电化学细胞系列首先由Luigi Galvani和Alessandro Volta研究 . 因此,它被称为Galvani细胞或伏尔蒂细胞. 两者都发现化学反应的能量形成. 通过伏特细胞的化学反应产生的能量是电能
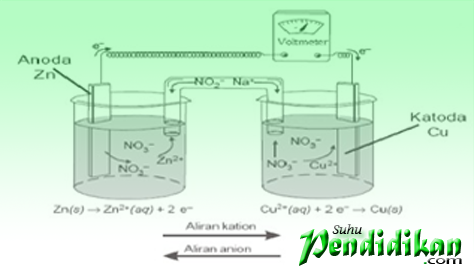
电极组成的伏尔塔细胞 (金属 & 铜) 电解质溶液 (ZnSO4和CUSO4), 和盐桥. 锌和铜金属充当电极. 两者都通过电压表连接. 发生氧化的电极称为阳极或负电极, 虽然减少的电极称为阴极或正电极
伏电池符号
•伏尔塔细胞以商定的方式表示 (对于Zn/Cu2+细胞)
Zn(s)|Zn2+(aq)║Cu2+(aq)|铜(s)
Redooks的示例
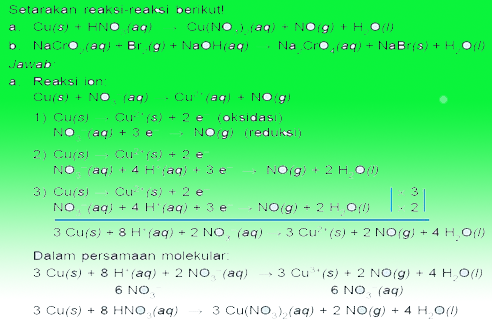
因此,氧化还原和电化学的语言, 希望有用
其他文章 :
- 溶液的界限 : 摩尔力, 摩尔和摩尔分数
- 几何公式和几何序列示例
- 病毒 : 结构, 分类, 形式, 病史的历史和理解和例子
氧化还原后和电化学反应 : 对问题的理解和示例首先出现在此页面上.